

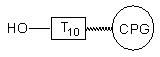
I
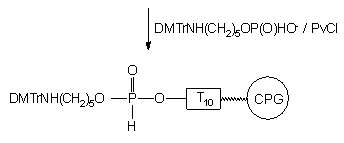
X
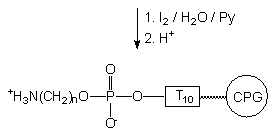
VI
Schemat 43
Często dyskutowana niedogodność tego podejścia wiąże się z koniecznością wcześniejszego przygotowania odpowiedniego H-fosfonianu aminoalkilowego. W niniejszej rozprawie niedogodność ta została w znacznej mierze ograniczona, gdyż w przeciwieństwie do znanych metod,10,54 synteza syntonu nienukleotydowego typu 182 oparta jest o proste, handlowe substraty bez konieczności ich wcześniejszego przygotowywania (str. *).
Synton 182d (0,2M roztwór w CH3CN-Py 1:1) przyłączyłem
do oligomeru I (Zdjęcie 5, linia A) stosując standardowe warunki
kondensacji metody H-fosfonianowej (0,3M roztwór PivCl w CH3CN-Py 1:1,
1,5 min.). Niezależnie od metody uzyskania oligomeru wykorzystywanego do
funkcjonalizacji, po utlenieniu, odblokowaniu i odtrytylowaniu otrzymywałem
5'-(5-aminopentylo)-fosforan oligonukleotydu VI (Zdjęcie 5, linia
B) jako praktycznie jedyny produkt.
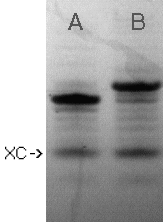
Zdjęcie 5
Tak więc, powyższe podejście jest szybkie i wydajne, w dużej mierze dzięki możliwości łatwego przygotowania H-fosfonianów typu 182. Biorąc pod uwagę fakt, że przyłączanie syntonu 182 odbywa się w standardowym cyklu syntetycznym kondensacji metody H-fosfonianowej, mogę polecać Wariant III jako efektywną metodę funkcjonalizacji oligonukleotydów związanych z podłożem stałym.
